如今席捲全球的 Omicron到底是一種怎樣的病毒?
2022年5月16日,Nature發表一篇關於新冠病毒 Omicron BA.2(新冠突變病毒奧密克戎的一種)突變株毒力的研究論文,首次在體內模型肯定了 BA.2的毒力確實低於之前的原始毒株。
這似乎也符合人們一直以來觀察到的情況:新的新冠突變株,一直在朝着越來越溫和的方向發展。
那麼,這會是最後一個新冠突變株嗎?
最新研究:BA.2毒力弱於原始毒株
Nature這篇最新研究來自東京大學和威斯康星大學的著名病毒學家、美國科學院院士 Yoshihiro Kawaoka,這也是迄今為止最為全面的在體內評估抗病毒療法(包括小分子藥物以及抗體)對 BA.2有效性的研究。
研究人員選取了在日本分離的 BA.2活病毒感染人源化 k18-hACE2小鼠和倉鼠,結果發現,在感染同樣劑量的病毒後,BA.2和 BA.1感染小鼠肺中和鼻中的感染性病毒滴度顯著低於新冠原始毒株感染(p
這一金標準結果證實了 Omicron的毒力確實低於原始野生型。而 BA.2和 BA.1感染後在肺和鼻中產生的病毒滴度則沒有觀察到顯著差異。
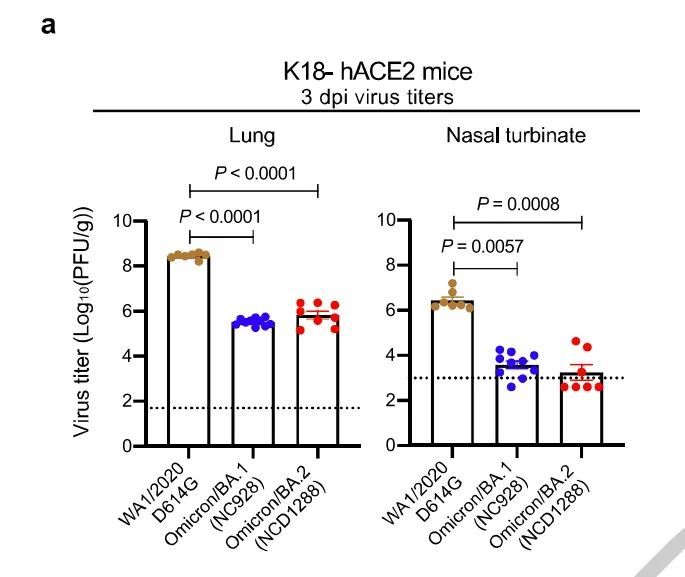
圖源:參考文獻1
PCR病毒載量檢測顯示, BA.2和 BA.1感染後的小鼠在肺和鼻中的病毒載量都低於新冠原始毒株,尤其在肺中顯著低於新冠原始毒株(p
「接種」了同樣劑量的病毒後,感染 BA.2和 BA.1的倉鼠鼻中和肺中檢測到的病毒滴度均低於原始毒株,尤其肺中降低更為明顯,感染 BA.2倉鼠鼻中檢測到的病毒滴度略低於 BA.1——實際上,BA.2感染倉鼠有一半沒有發展成肺部感染。
研究進一步發現,原始毒株,BA.2和 BA.1感染後的血清缺乏交叉中和——這與在真實世界人類感染不同新冠突變株時所觀察到的現象一致。
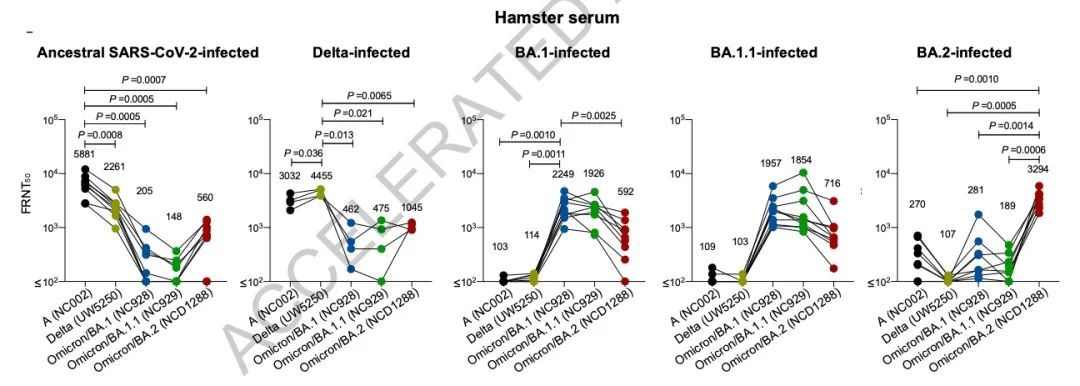
圖源:參考文獻1
研究還評估了疫苗接種者血清對原始毒株、Delta以及三種 Omicron突變病毒 BA.1、BA.1.1、BA.2的活病毒中和活性(FRNT),結果發現,3劑輝瑞/BioNTech新冠疫苗 BNT162b2接種後14天,對 BA.1和 BA.2的中和活性顯著低於原始毒株。不過,在接種1個月後,對 BA.2的中和滴度 FRNT50從631上升到2029。
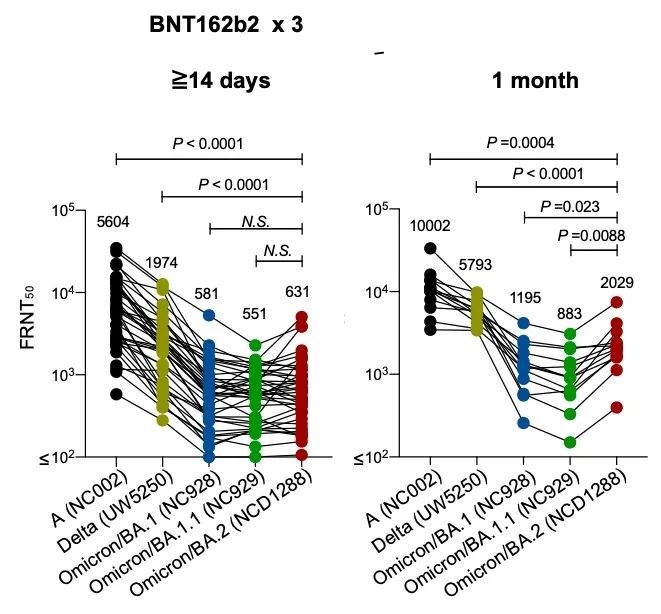
圖源:參考文獻1
此外,研究人員對病毒感染倉鼠進行了抗體治療,結果發現 REGN10987/REGN10933(再生元 REGEN-COV),COV2-2196/COV2-2130(阿斯利康 AZD7442)和 S309(一種 SARS康復者抗體)對 BA.2感染有一定治療效果。
而在抗病毒藥物方面,默沙東的 Molnupiravir、輝瑞 Paxlovid中主要成分 Nirmatrelvir和新蛋白酶抑制劑 S-217622均可以在肺中完全抑制病毒,其中 S-217622可顯著抑制鼻中病毒複製。
新冠突變株,會越變越弱嗎?
多項實驗室研究和真實世界情況都在驗證,與原始毒株和此前多種突變株相比,Omicron是一種傳播力更強,而致病力更低的突變株。
這是否意味着,新冠病毒的突變會越變越溫和?
一些觀點認為,隨着新冠的持續突變,新的變體越來越像流感,或成為一種季節性、地方性的疾病。然而,一篇發表於 Nature Reviews Microbiology的評論文章提出了反對觀點。
圖源:參考資料2
來自牛津大學和歐盟聯合研究中心的三名科學家認為,Omicron的嚴重程度較低是一個巧合,持續快速的抗原進化(antigenic evolution)可能會帶來新的變體,這些變體可能會出現免疫逃逸並導致嚴重的疾病。
長久以來,有不少人認為,病毒會出於持續傳播的目的而削弱致病性/致命性,進化得更加溫和。而這篇評論文章提出,與承受強大進化壓力的免疫逃逸能力和傳播力不同,病毒的毒力通常只是一種進化的「副產品」。
病毒進化的目的在於最大限度地提高傳播能力,而這也可能會導致毒力的上升。例如通過提高病毒載量促進傳播,依然會引發更嚴重的疾病。
不僅如此,如果病毒帶來的症狀主要在感染後期出現,那麼,毒力在病毒傳播過程中造成的危害也將非常有限——如流感病毒、愛滋病毒和丙型肝炎病毒等等,在造成嚴重後果之前,它們有充分的時間進行傳播。
在這樣的情況下,我們很難通過 Omicron的較低毒力來預測新冠突變株的發展趨勢,未來出現傳播力增加且毒力也增加的新冠突變株也是完全有可能的。
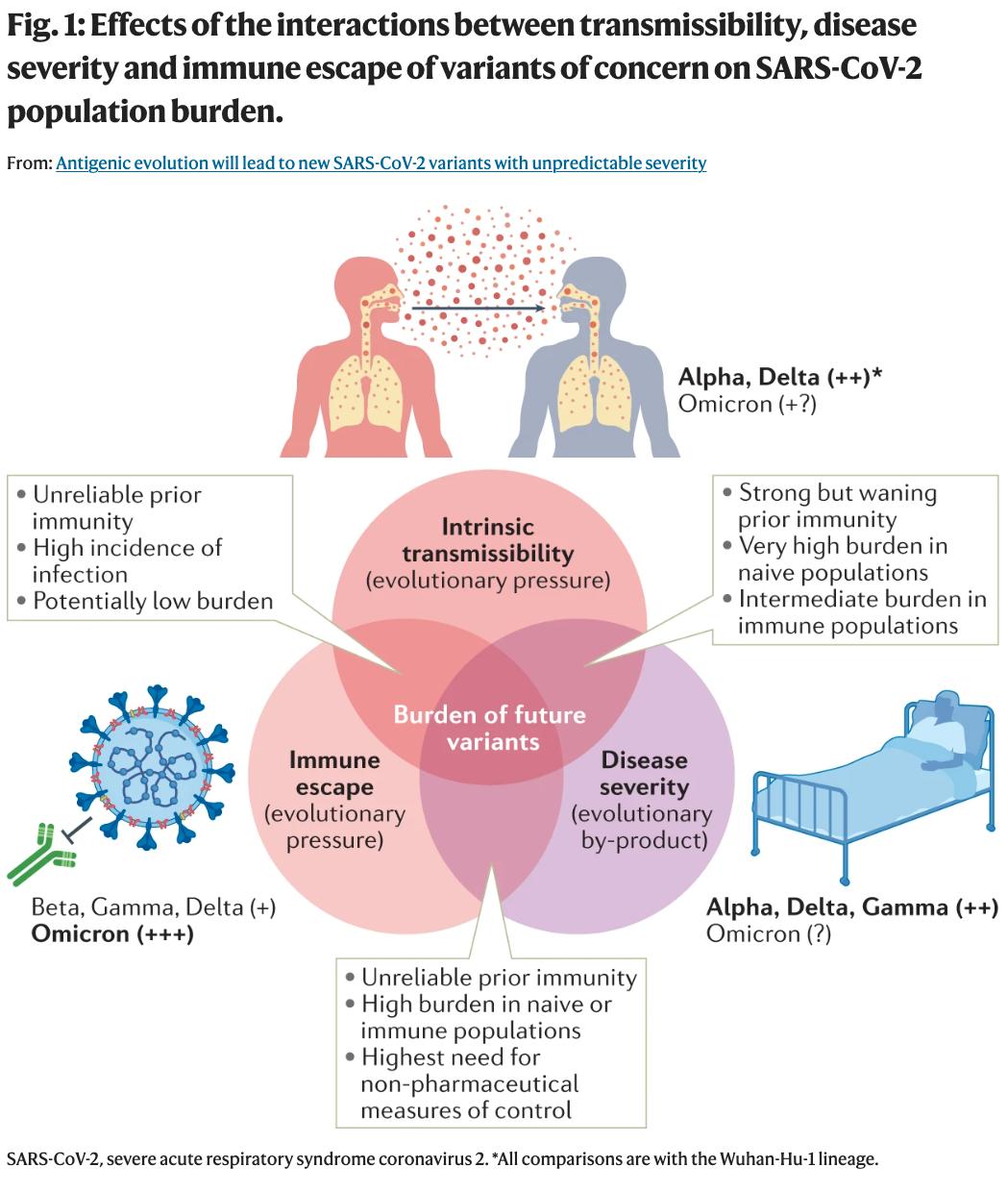
圖源:參考資料2
那麼,我們通過廣泛的疫苗接種來建立群體免疫,是否有可能減緩未來新冠的傳播呢?
Nature子刊評論文章對此持有不同意見。
回顧新冠大流行以來的幾種主要變體,早期,它們通過增加傳播力來提高自己的有效繁殖數 Rt,從而佔據主要流行地位——Alpha和 Delta的傳播力都比前一個變體要高出50%。
然而如今,新冠疫苗的推廣和既往感染已經讓人群具有了相當的免疫力,對此,病毒可能不僅僅要提高傳播力,還需要不斷的提高免疫逃逸能力,來繞過已經建立的免疫屏障,重新感染更多人。
這也就是所謂的突破性感染。
Omicron的流行證實了這點,新冠可以在相對較短的時間就進化出極強的免疫逃逸能力,並迅速在已經接種了新冠疫苗的人群中傳播,取代 Delta成為了主流毒株。
因此,隨着人群免疫水平的提升,新冠病毒的進化策略可能會更加趨向於提高免疫逃逸能力,增加再感染風險,並可能增加再感染的疾病嚴重程度。
下一個突變,能被預測嗎?
Omicron不會是新冠的最後一個突變株,那麼,下一個突變株將從哪裏來?又會在什麼時候來?
從 Alpha、Delta到 Omicron的流行過程中,我們常常忽視了一個非常關鍵的信息——這些主流突變株的更迭實際上並不是「線性」的。
流行病學家 Adam Kucharski在個人 Twitter中提到,在以往的季節性冠狀病毒和流感病毒的進化過程中,由於新的變體總是在逃逸人體對此前變體產生的免疫力,於是,我們觀察到了一種明顯的「線性」進化趨勢。
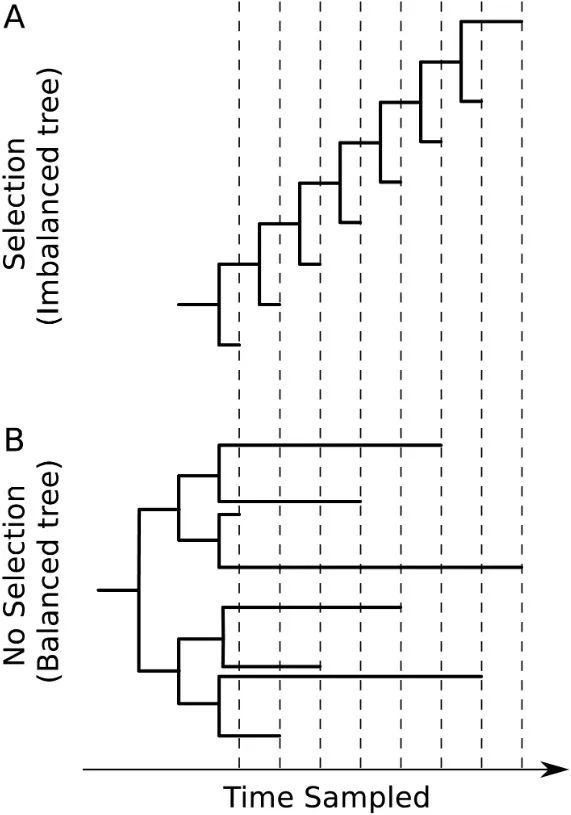
「線性」進化趨勢如上圖
圖源:參考資料3
這在季節性冠狀病毒229E、季節性流感病毒 A/H3N2、和曾在2009年引發大流行的甲型 H1N1p流感病毒的進化樹上都有體現。

甲型 H1N1p流感病毒的進化樹
圖源:參考資料4
然而,截至 Omicorn流行時,我們暫時還沒有觀察到新冠病毒呈現出這種「線性」進化趨勢。

圖源:參考資料5
Delta不是從 Alpha的基礎上進化而來的,Omicron也不是從 Delta的基礎上進化而來的。我們需要向前溯源到很久以前才能找到這些突變株的共同祖先,這也意味着,新冠病毒的突變更加隨機且難以預測。
5月10日,Science網站首頁發佈一則新聞報道,標題為《Omicron新亞型是免疫逃逸大師》,在這篇報道中,新發傳染病專家王林發提出,根據 Omicron毒株的免疫學特徵,建議將其定義為 SARS-CoV-3,即一種與 SARS-CoV-2完全不同的病毒。
而目前,Omicron的一系列子變體也正在引發越來越多的關注。
BA.2已經在全球至少68個國家佔據主要流行地位,而與此同時,BA.4、BA.5已經成為了南非的主要變體。
據葡萄牙國立衛生院估計,截至2022年5月8日,BA.5已佔陽性病例的約37%,按照這樣的增長率,到2022年5月22日,BA.5就將成為葡萄牙的主要變體。
歐洲疾控中心在5月13日正式將 BA.4和 BA.5從「感興趣的變體」升級成為「關注的變體」,儘管暫時沒有觀察到 BA.4和 BA.5在致病力方面與 BA.2有何變化,但一些體外研究表明,這兩種變體都可逃逸由 BA.1帶來的免疫保護。
2022年5月16日,中國疾控中心周報中通報了我國大陸首例 Omicron BA.2.12.1,為境外輸入。與此同時,根據美國疾控中心檢測到的數據,BA.2.12.1正在以驚人的速度流行。5月8日到5月14日這一周,美國報告的病例中,BA.2.12.1佔比已經達到了47.5%。
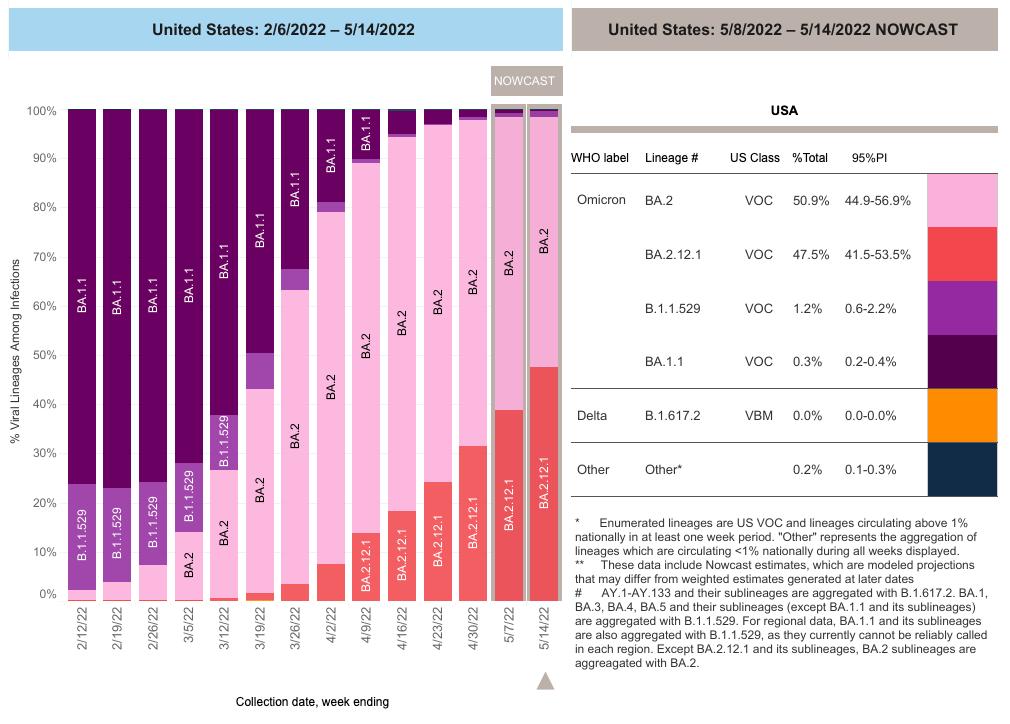
圖源:美國 CDC
值得注意的是,BA.4、BA.5、BA.2.12.1三種新亞型都攜帶一個和 BA.2一樣的突變位點:L452突變。
L452蛋白是新冠 S蛋白受體結合結構域的一部分,該結構域也是保護性抗體的重要作用點,這一突變可能有助於增加其免疫逃逸能力。
隨後北京大學免疫學家曹雲龍等進行的中和抗體試驗發現,曾感染 BA.1受試者血清對於 BA.4、BA.5、BA.2.12.1這三種新亞型的中和能力很弱,而此前感染過 SARS且完成新冠疫苗接種的受試者血清對新亞型的中和能力更差。
這些迅速的變化給疫苗研發和防疫政策制定都來了諸多挑戰。儘管不斷有疫苗研發廠商宣佈在對新的突變株進行研發,但出成果的速度依然很難超過新冠病毒疊代更新的速度。
對此,王林發表示,針對不同毒株的廣泛單克隆抗體藥物可能是後續更好的應對方向。
王林發表示,這種手段能夠為脆弱人群提供保護,比如免疫能力低下無法對疫苗產生效果的人群。他提出,保護這一群體至關重要,因為許多研究人員懷疑免疫系統缺陷的病人,無法清除病毒,在長期感染期間可能出現更多地新變異。
Natrue子刊的評論文章同樣也提到了這一點。文章認為,除了探索抗原逃逸與疾病嚴重程度的關係之外,我們還需要仔細研究產生高度抗原性差異變體的機制及其出現的環境。
這些環境可能是患有慢性疾病或存在免疫缺陷的個人,也有可能是存在免疫缺口的特定地區,甚至有可能是於人類社會關聯較密切的動物群體。只有了解這些因素,我們才能更準確地評估未來可能會面臨的風險,並為此做好計劃和準備。
















