新冠肺炎和流感都是傳染性呼吸系統疾病,二者有一些相似症狀,但它們是由不同病毒引起的,並且罹患重症的人群特徵和治療方式都存在一些差異。疫苗接種是預防感染的有效途徑,新冠病毒和流感病毒並不相同,在疫苗效力方面有各自的作用方式。最近的研究表明,接種流感疫苗降低了90%的新冠重症。我們必須了解新冠病毒和流感病毒之間的區別,以更好地保護自己。
2022年5月16日, Nature發文表示流感疫苗可以降低新冠感染風險,特別是在新冠重症防護方面,具有90%的效力(圖1)[1]。如果我們提前知道流感或者其他疾病的疫苗可以提供針對新冠病毒的防護,那麼即使只是在很短的時間內提前知道,也可以降低未來新冠大流行造成的死傷,挽救數百萬人的生命,為開發新冠疫苗留出時間。

圖1相關報道(圖源:Nature)
2022年5月9日,多哈威爾康奈爾醫學中心研究團隊在預印本平台medRxiv發表題為「 Effectiveness of influenza vaccination against SARS-CoV-2 infection among healthcare workers in Qatar」的研究成果(圖2)[2]。研究發現與最近未接種流感疫苗的人相比,接種流感疫苗的人在接下來的幾個月內患新冠重症的可能性降低了近90%。

圖2研究成果(圖源:medRxiv)
此項研究由傳染病流行病學家Laith Jamal Abu-Raddad領導,並分析了2020年9月17日至2020年12月31日之間(新冠疫苗接種之前,流感疫苗接種之後的時期),卡塔爾30774名醫務人員的健康記錄。數據樣本的中位年齡為36歲,對照組中位年齡為35歲,流感疫苗接種和PCR(Polymerase Chain Reaction)檢測之間的中位持續時間為43天(圖3)。
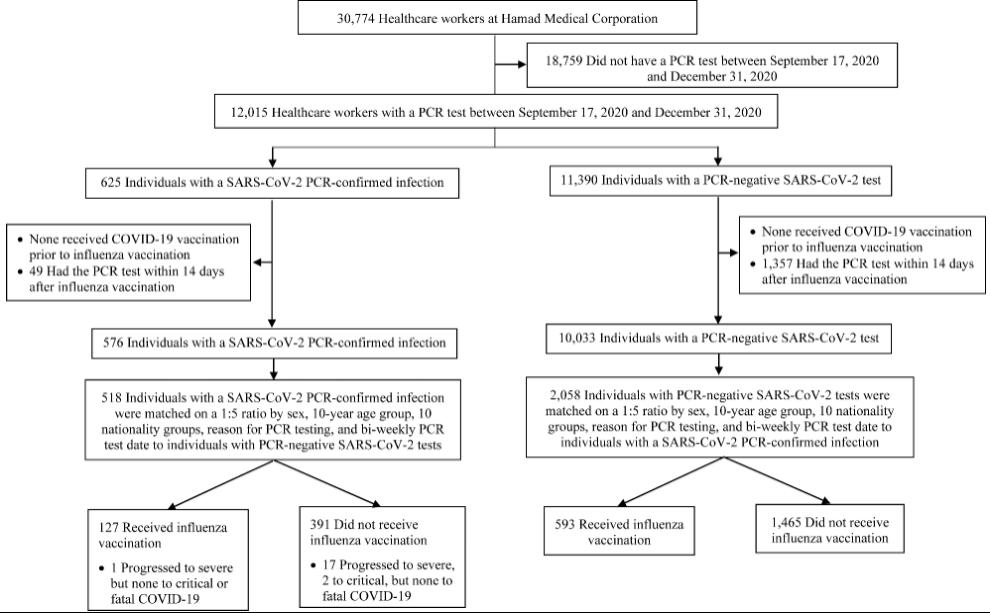
圖3調查流感疫苗對SARS-CoV-2感染有效性的人群選擇路徑(圖源:[2])
通過對數據結果分析,得到以下結論:
1、接種流感疫苗14天後對新冠病毒的防護有效性為29.7%;
2、流感疫苗對任何嚴重、危急或致命新冠症狀的有效性為88.9%;
3、流感疫苗接種與SARS-CoV-2感染風險和COVID-19嚴重程度的顯著降低有關;
4、流感疫苗對新冠的防護效力時間約為六周。
瑞士巴塞爾大學的流行病學家Günther Fink表示:「我們之前在巴西的研究結果表明,流感疫苗接種與COVID-19住院患者的死亡風險降低有關。卡塔爾的此項分析降低了其他發現相同聯繫的研究只是僥倖的可能性。」
荷蘭奈梅亨拉德堡德大學醫學中心的傳染病專家Mihai Netea說:「這是一個重要的證據,流感疫苗不僅與減少SARS-CoV-2感染有關,而且與疾病嚴重程度有關,這一觀察強烈表明這種保護是真實存在的。但是,我不認為流感疫苗對新冠的防護效力會持續很長時間,可能也就持續六個月到兩年。目前尚不完全清楚為什麼由滅活流感病毒組成的流感疫苗也能預防新冠肺炎。疫苗訓練免疫系統以識別特定病原體,但它們也增強了廣泛作用的抗病毒防禦能力,Laith Jamal Abu-Raddad在流感疫苗接種者身上發現了這種反應的跡象。」
流感病毒與新冠病毒有何異同?
病毒是一種在活細胞內寄生並以複製方式增殖的非細胞型生物。不同病毒侵入細胞的方式不同,但大都需要通過結合細胞表面特定的受體蛋白或脂質結構來實現細胞內化,從而啟動入侵程序和感染宿主細胞。因此揭示病毒結合和內化侵入細胞的具體過程及機制有助於從源頭上開發靶向藥物或疫苗。
流感病毒按照核蛋白的抗原性,可分為甲(A)、乙(B)、丙(C)、丁(D)四型。人流感主要是A型和B型流感病毒引起的,C型流感病毒只引起人類不明顯的或輕微的上呼吸道感染,D型流感病毒的宿主主要是牛。流感病毒屬於正粘病毒科,是一種包膜病毒,膜上鑲嵌着3類膜蛋白:血凝素(Hemagglutinin,HA)、神經氨酸酶(Neuraminidase,NA)和膜蛋白M2(Membrane protein2,M2)。HA以同源三聚體的形式存在。
HA水解後形成輕鏈和重鏈兩部分,其中重鏈負責病毒與細胞的結合,而輕鏈則協助病毒膜與內吞體膜的半融合。NA是蘑菇狀的四聚體糖蛋白,具有水解唾液酸的活性,能幫助病毒從宿主細胞中釋放。膜蛋白M2具有離子通道和調節膜內pH的作用。此外,基質蛋白M1構成病毒的外殼骨架,與病毒最外層的包膜緊密結合,起到保護病毒核心和維持病毒空間結構的作用。病毒的遺傳物質是單股負鏈RNA與核蛋白摺疊在一起(電視劇)形成的病毒核糖核蛋白複合物(圖4)。
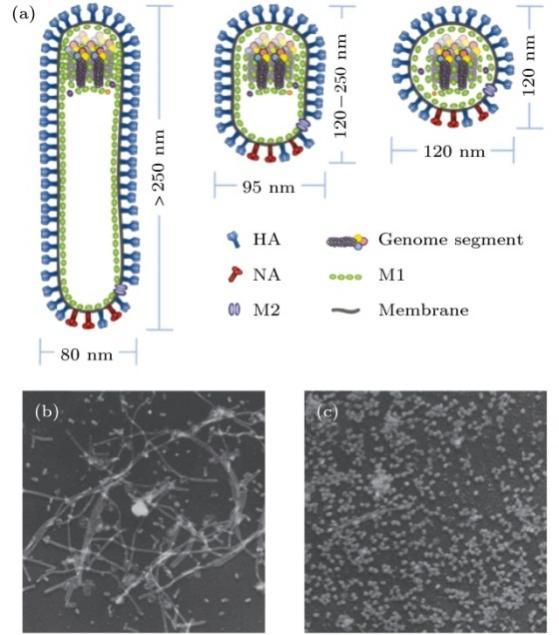
圖4流感病毒結構與形狀(圖源:[3])
冠狀病毒是自然界廣泛存在的一大類病毒,僅感染脊椎動物,最早是從雞身上分離出來的。冠狀病毒粒子直徑約為60-220 nm,表面有3種糖蛋白:刺突糖蛋白,小包膜糖蛋白,膜糖蛋白,少數還含有血凝素糖蛋白(圖5)。冠狀病毒的核酸為線性單股正鏈RNA,5』端具有甲基化帽狀結構,3』端具有polyA尾,類似於真核mRNA,自身就可以發揮翻譯模版作用,基因組全長27-32 kb,是目前已知RNA病毒中基因組最大的病毒。
國際病毒分類委員會將其分為4個屬,即α、β、γ及新假定的δ冠狀病毒屬。新冠病毒是一種β屬冠狀病毒,有很強的傳染能力。目前已經檢測出新冠病毒的全基因組序列及病毒與細胞結合的蛋白等,但對於它通過何種路徑侵入並感染細胞的機制尚不清楚。
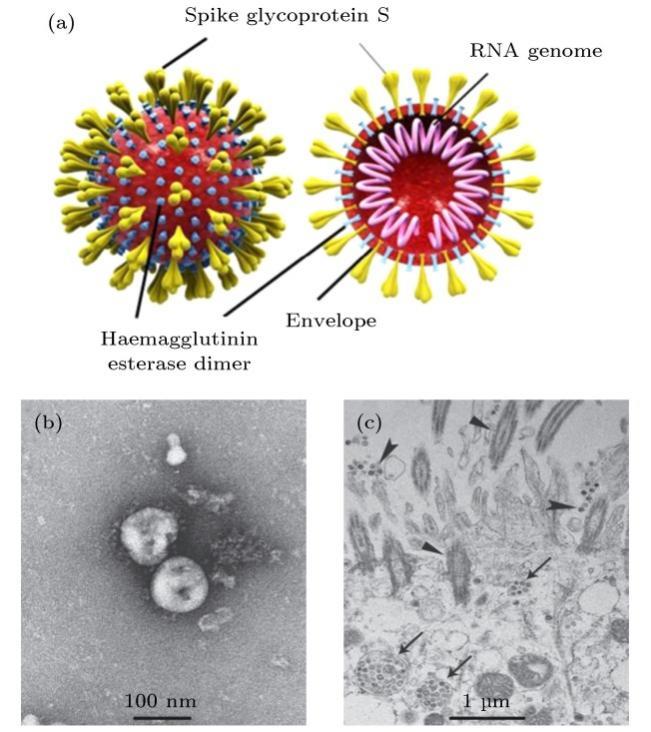
圖5新冠病毒結構與透射電子顯微圖像(圖源:[3])
流感病毒與SARS-CoV-2都是通過配體受體相結合的方式吸附至細胞表面,經細胞內蛋白水解酶的作用將HA和S蛋白活化形成兩個亞基,分別負責病毒與宿主細胞的結合及介導膜融合過程。流感病毒結合至細胞受體後需要多種細胞因子的參與才能實現內吞,而有研究表明新冠病毒同樣可能利用細胞內的某些促吸附因子,例如與細胞糖蛋白的結合,來增強其感染性。
流感病毒與新冠病毒在對細胞作用的機理上存在一些相似之處,因此利用流感病毒的研究方法開展對新冠病毒與細胞作用的研究是一條潛在的途徑,流感疫苗對新冠的防護也就不難理解。